Industries alimentaire et pharmaceutique
Lois et réglementations relatives à la traçabilité applicables aux industries alimentaire et pharmaceutique dans le monde
Outre les réglementations internationales telles que l’ISO 9000/9001 relative au management de la qualité dans toute industrie, l’HACCP dédié à l’industrie alimentaire et les BPM destinées à l’industrie pharmaceutique, chaque pays dispose de ses propres lois et réglementations en matière de traçabilité.
Face à la mondialisation croissante, il est aujourd’hui essentiel de comprendre les lois et réglementations étrangères et d’appliquer les mesures qu’elles préconisent pour assurer la traçabilité. Cette page présente les lois et réglementations applicables aux industries alimentaire et pharmaceutique dans divers pays, incluant les Principes généraux de la législation alimentaire dans l’UE et le Bioterrorism Act (Loi sur le bioterrorisme) aux États-Unis.
HACCP
HACCP est un acronyme signifiant Hazard Analysis Critical Control Points (système d’analyse des risques — points critiques pour leur maîtrise). Il s’agit d’une méthode de contrôle d’hygiène alimentaire, basée sur le rapport publié en 1993 par la Commission du Codex Alimentarius, une organisation commune à l’Organisation des Nations Unies pour l'alimentation et l'agriculture (FAO) et l’Organisation Mondiale de la Santé (OMS), appliquée partout dans le monde.
L’HACCP désigne une méthode de contrôle de la sécurité qui consiste à analyser scientifiquement les risques potentiels relatifs à la salubrité d’un aliment, tels que le risque d’empoisonnement, d’un bout à l’autre de la chaîne alimentaire, de la réception des matières premières à l’expédition, en passant par la fabrication et le traitement, puis à identifier les points de contrôle critiques pour réduire ou éliminer ces risques. Au Japon, l’HACCP a été institué à travers l’amendement Gestion intégrée d'hygiène au processus de la fabrication, publié en 1995.
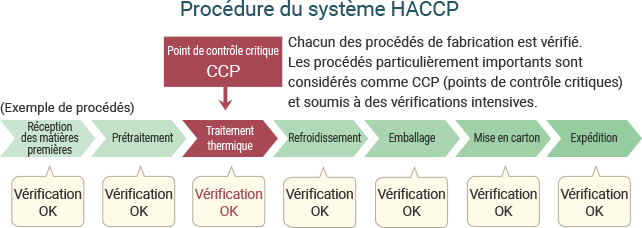
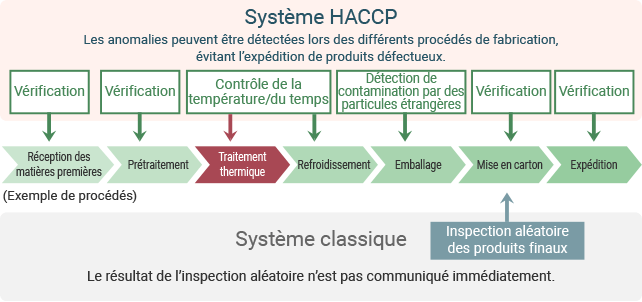
Différences entre l’HACCP et le contrôle d’hygiène classique
Dans le cadre d’un contrôle d’hygiène classique, les normes applicables aux installations/équipements et aux méthodes de traitement des aliments sont spécifiées puis les produits finaux sont contrôlés. Le système HACCP préconise d’analyser les risques à chaque procédé de fabrication, de réaliser des vérifications intensives lors des procédés importants et d’effectuer un contrôle/une inspection sur la base d’une norme spécifiquement dédiée à chaque procédé. Les contre-mesures prises tout au long de la chaîne permettent de prévenir les empoisonnements alimentaires et contaminations par des particules étrangères avant que ne se produise un problème, renforçant ainsi la sécurité.
Principes de traçabilité alimentaire unifiés dans l’UE : Principes généraux de la législation alimentaire
Avant le problème de l’ESB (maladie de la vache folle) survenu en Europe en 1996, l’UE ne disposait pas de principes unifiés concernant la législation alimentaire. N’existait alors qu’un ensemble de lois établies individuellement pour chaque cas. Cet état de fait a été mis en lumière par la crise de l’ESB, qui a conduit à l’établissement d’une réglementation unifiée, appelée Principes généraux de la législation alimentaire et promulguée en 2002, qui pose les principes généraux et prescriptions générales de la législation alimentaire, créé l’Autorité européenne de sécurité des aliments et définit les procédures relatives à la sécurité alimentaires (CE) N°178/2002.
Spécification complète, jusqu’aux éléments des registres de traçabilité
En matière de traçabilité, l’article 18 des Principes généraux de la législation alimentaire stipule le principe suivant : la traçabilité des denrées alimentaires, des aliments pour animaux, des animaux producteurs de denrées alimentaires et de toute autre substance destinée à être incorporée ou susceptible d'être incorporée dans des denrées alimentaires ou des aliments pour animaux est établie à toutes les étapes de la production, de la transformation et de la distribution.
Il est spécifié que les acteurs de la chaîne alimentaire doivent tenir les informations suivantes à disposition des autorités compétentes, à la demande de celles-ci. Les principes recommandent également de collecter et conserver des informations plus détaillées sur le produit, telles que la quantité.
| Fournisseur | Client |
|---|---|
| Nom | Nom |
| Lieu | Lieu |
| Type de produit fourni au client | Type de produit fourni par le fournisseur |
| Date de transaction et de livraison | Date de transaction et de livraison |
Loi relative à la traçabilité alimentaire aux États-Unis : Bioterrorism Act
Aux États-Unis, la traçabilité alimentaire est régie par le Bioterrorism Act (The Public Health Security and Bioterrorism Preparedness and Response Act of 2002 (Loi américaine de 2002 sur la sûreté de la santé publique et sur la prévention du bioterrorisme)).
Le Bioterrorism Act impose la mise en œuvre obligatoire de mesures telles que l’enregistrement des installations pour produits agro-alimentaires, la notification préalable des importations, l’établissement et la tenue de registres et la détention administrative. Les mesures de la loi relatives à la traçabilité sont liées à la tenue de registres.
Il est exigé des opérateurs qui fabriquent, transforment, conditionnent, transportent, distribuent, reçoivent, stockent ou importent des produits alimentaires aux États-Unis qu’ils établissent et tiennent des registres. La gestion des liens entre les procédés une étape en aval et une étape en amont, telle que décrite dans la section « Mettre en place un système d’identification », est requise par la loi. De plus, si un produit est soupçonné de présenter une menace pour la santé humaine ou animale, les opérateurs concernés devront mettre tous les registres et autres informations à la disposition de la Food and Drug Administration (FDA - administration américaine chargée des aliments et des médicaments).
Durée de conservation des registres
Le Bioterrorism Act définit la durée de conservation en fonction de la nature périssable du produit alimentaire :
| Catégorie | Non-transporteurs | Transporteurs |
|---|---|---|
| Produits présentant un risque élevé de détérioration dans une période de 60 jours | 6 mois | 6 mois |
| Produits présentant un risque élevé de détérioration après un minimum de 60 jours, mais dans une période de 6 mois | 1 an | 1 an |
| Produits présentant un risque élevé de détérioration après 6 mois | 2 ans | 1 an |
| Produits alimentaires pour animaux, y compris les animaux domestiques | 1 an | 1 an |
Réglementation relative à la traçabilité applicable à l’industrie pharmaceutique en Chine : Code de gestion des médicaments
Le code de gestion des médicaments est un système administré par la China Food and Drug Administration (CFDA), autorité chargée de garantir la sécurité des aliments et des médicaments, pleinement en vigueur depuis 2016. Les opérateurs souhaitant commercialiser des médicaments en Chine doivent obtenir au préalable une autorisation et un code de gestion des médicaments auprès de la CFDA, et intégrer ces informations sous la forme d’un code-barres.
Le code de gestion des médicaments a été introduit en 2012 à des fins de prévention de l’utilisation incorrecte de médicaments, de mise en œuvre de la traçabilité et d’amélioration de la distribution. Bien que son application soit jusqu’ici limitée, toutes les sociétés, incluant les opérateurs étrangers, sont tenues de mettre en pratique le système depuis 2016. Il est obligatoire d’inscrire le code-barres sur une étiquette ou directement sur l’extérieur de l’emballage de chaque produit et le cas échéant de chaque dose individuelle.

Configuration du code de gestion des médicaments

Les codes sont composés de 20 caractères numériques, intégrés sous la forme de codes-barres Code128C.
| 8 | 123456 | 123456789 | 1234 |
| 1 | 2 | 3 | 4 |
- 1. Nombre fixe, 1 caractère, « 8 »
- 2. Code du produit, 6 caractères, code d’article attribué à chaque article ou emballage, fourni par l’autorité administrative (China Drug Electronic Supervision and Administration Network - Réseau chinois de gestion et de supervision électronique des médicaments)
- 3. Numéro de série, 9 caractères, numéro assigné à chaque produit d’une société de fabrication
- 4. Code de vérification, 4 caractères, données de vérification